1. Vị trí và cấu tạo

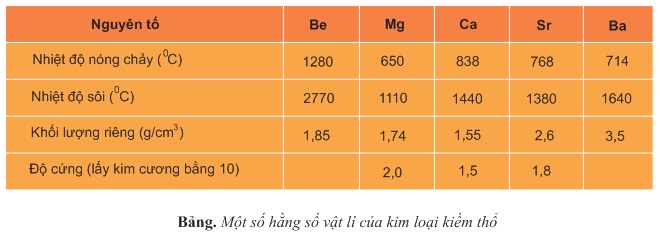
2. Tính chất vật lý
Kim loại kiềm thổ có nhiệt độ nóng chảy, nhiệt độ sôi và độ cứng cao hơn kim loại kiềm nhưng vẫn tương đối thấp (trừ beri). Khối lượng riêng tương đối nhỏ.
3. Tính chất hóa học
– Các kim loại kiềm thổ đều có tính khử mạnh nhưng yếu hơn so với kim loại kiềm.
– Tính khử tăng dần từ Be đến Ba.
M – 2e → M2+
3.1. Tác dụng với phi kim
a. Tác dụng với oxi
Kim loại kiềm thổ phản ứng với oxi tạo ra oxit hoặc peoxit
VD: 2Mg + O2  2MgO
2MgO
b. Tác dụng với halogen
M + X2 → MX2
3.2. Tác dụng với dung dịch axit
Là nhóm kim loại hoạt động hóa học mạnh nên kim loại kiềm thổ có phản ứng với axit
– Với axit HCl, H2SO4 loãng: khử H+ thành H2
Ca + 2HCl → CaCl2 + H2↑
– Với axit HNO3, H2SO4 đặc
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
4Mg + 5H2SO4 (đặc) → 4MgSO4 + H2S + 4H2O
3.3. Tác dụng với nước
– Ca, Sr, Ba tác dụng với nước ở nhiệt độ thường tạo dung dịch bazơ
Ba + 2H2O → Ba(OH)2 + H2↑
– Be không phản ứng với nước ở nhiệt độ thường, Mg phản ứng chậm.
4. Điều chế kim loại kiềm thổ
Phương pháp cơ bản để điều chế kim loại kiềm thổ là điện phân muối nóng chảy của chúng
MCl2  M + Cl2
M + Cl2